19/Septiembre/2014
Regla del OctetoEstablece que los átomos de los elementos se enlazan unos a otros en el intento de completar su valencia.
La denominación regla del octeto surgió en razón de la cantidad establecida de electrones para la estabilidad de un elemento, o sea, el átomo queda estable cuando presenta en su capa de valencia 8 electrones.
Para alcanzar tal estabilidad sugerida por la octeto, cada elemento precisa ganar o perder (compartir) electrones en los enlaces químicos, de esa forma ellos adquieren 8 electrones en la capa de valencia.
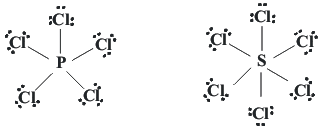
Regla de HUND
Es un método empírico utilizado para el llenado de orbitales que posea igual energía, así podemos decir que existen tres orbitales tipo P, cinco orbitales atómicos tipo D, y siete tipo F.
En ellos se van colocando los electrones con espines paralelos en la medida de lo posible.
La partícula analizada será más estables (tendrá menor energía), cuando los electrones se encuentren en modo desaparecido, con espines colocados paralelamente, en cambio poseerá mayor energía cuando los electrones se encuentren apareados, es decir, los electrones colocados de manera antiparalela o con espines de tipo opuestos.
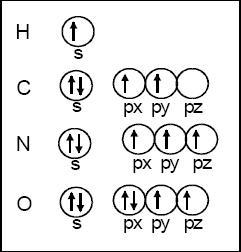
Tabla de Aufbau
El principio de Aufbau contiene una serie de instrucciones relacionadas a la ubicación de electrones en los orbitales de un átomo.
Los orbitales se "llenan" respetando la regla de Hund, que dice que ningún orbital puede tener dos orientaciones del giro del electrón sin antes de que los restantes números cuánticos magnéticos de la misma subcapa tengan al menos uno. Se comienza con el orbital de menor energía.
Primero debe llenarse el orbital 1s (hasta un máximo de dos electrones), esto de acuerdo con el número cuántico 1. Seguido se llena el orbital 2s (también con dos electrones como máximo).
La subcapa 2p tiene tres orbitales degenerados en energía denominados, según su posición tridimensional, 2px, 2py, 2pz. Así, los tres orbitales 2p puede llenarse hasta con seis electrones, dos en cada uno. De nuevo, de acuerdo con la regla de Hund, deben tener todos por lo menos un electrón antes de que alguno llegue a tener dos.


No hay comentarios:
Publicar un comentario